Návštěvnost dne 25. února 2026 byla — 484 927 unikátních návštěvníků !
Návštěvnost dne 26. února 2026 byla — 479 665 unikátních návštěvníků !
Návštěvnost dne 5. března 2026 byla — 475 445 unikátních návštěvníků !
Glukóza
Z Multimediaexpo.cz
| D-glukosa | |
| Aldehydická forma (ve Fischerově projekci) Strukturní vzorec Hemiacetalová forma (standardní strukturní vzorec) Strukturní vzorec | |
| Systematické jméno | 6-(hydroxymethyl)oxan-2,3,4,5-tetrol (hemiacetalová forma) |
| Registrační číslo CAS | 50-99-7 (D-glukosa) 921-60-8 (L-glukosa) |
| Sumární vzorec | C6H12O6 |
| Molární hmotnost | 180,155 g/mol |
| Teplota tání | 146 °C (bezvodá, α-D-anomer) 150 °C (bezvodá, β-D-anomer) 83 °C (monohydrát) |
| Teplota varu | (rozklad) |
| Hustota | 1,56 g/cm3 |
| Rozpustnost ve vodě | 1200 g/l |
| Specifická otáčivost | +106º (α-anomer) +22.5º (β-anomer) +52.5º (anomery v rovnováze) (D, 20 °C] |
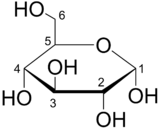
Glukosa, mimo chemii podle PČP glukóza (z řec. γλυκύς, tj. glykys, česky sladký nebo γλευκος, gleukos, česky mošt, sladké víno), v běžné řeči označovaná jako hroznový cukr nebo krevní cukr, je jedním z monosacharidů ze skupiny aldohexos. V chemických vzorcích oligosacharidů a polysacharidů se značí symbolem Glc. V čistém stavu je glukosa bílá krystalická látka sladké chuti.
Obsah |
Výroba
D-glukosa se může připravit krystalizací z rostlinných šťáv, zejména z hroznů vinné révy, ale hlavní metodou její výroby je kyselá nebo enzymatická hydrolýza rostlinného škrobu, v Česku především bramborového.
Chemické vlastnosti
Glukosa existuje ve dvou enantiomerech a to jako D-glukosa (vyskytující se v přírodě), nazývaná též dextrosa a její zrcadlový obraz, L-glukosa. Ty se svými chemickými a fyzikálními vlastnostmi neliší, s výjimkou toho, že jejich vodný roztok stáčí rovinu polarizovaného světla opačným směrem. V živých organismech jsou však nezaměnitelné.
Vzhledem k přítomnosti aldehydické skupiny patří glukosa k redukujícím sacharidům, tj. např. redukuje soli dvojmocné mědi na jednomocné, což se v minulosti užívalo ke kvalitativnímu i kvantitativnímu stanovení cukru v roztoku (například v moči). Přitom se aldehydická skupina D-glukosy se mění na karboxylovou a vzniká kyselina D-glukonová. Při použití silnějších oxidačních činidel, jako např. kyseliny dusičné se oxiduje též primární alkoholická skupina na opačném konci molekuly též na karboxylovou skupinu za vzniku kyseliny D-glukarové. Zoxiduje-li se pouze primární alkoholická skupina na posledním uhlíku (s lokačním číslem 6), vzniká kyselina D-glukuronová.
Redukcí glukosy např. hydrogenací vodíkem za přítomnosti katalyzátorů se naopak redukuje aldehydická skupina na primární alkoholickou skupinu a vzniká D-glucitol, známější pod názvem sorbitol (sorbit), používaný jako umělé sladidlo pro diabetiky.
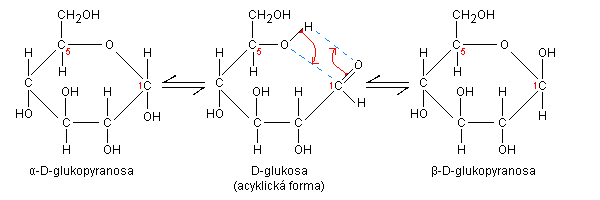
V roztoku přechází glukosa do cyklické hemiacetalové formy s šestičlenným kruhem (pyranosa), která v rovnovážném stavu za laboratorní teploty 20 °C obsahuje dva anomery, lišící se orientací hemiacetalového hydroxylu: 36 % α-glukopyranosy a 64 % β-glukopyranosy.
- 6 CO2 + 6 H2O + hν → C6H12O6 + 6 O2,
přičemž vzniká kyslík. Přesně opačným procesem je proces, kterým organismy rostlin a živočichů odbourávají („spalují“) D-glukosu na původní látky a získávají tak potřebnou energii. Obecně o chemických vlastnostech a reakcích viz též heslo aldosa.
Výskyt v přírodě
Čistá D-glukosa se nachází v rostlinách jako jeden z produktů fotosyntézy a představuje pro rostliny zásobu energie. Hromadí se především v plodech. Kromě toho je podjednotkou řady přírodních oligosacharidů, např. maltosy, sacharosy, galaktosy aj. a polysacharidů, např. škrobu nebo glykogenu. Obecně se tyto glukózové sacharidy nazývají glukany. Je také součástí mnoha heteroglykosidů, vyskytujících se v rostlinách. Je také přítomna v krvi živočichů, i v některých živočišných produktech, zejména v medu. Člověk s cukrovkou má více glukózy v moči.
Fyziologický význam
D-Glukosa je pro existenci našeho organizmu nezbytná. Je to nejrychlejší a nejzákladnější zdroj energie pro lidské tělo, obzvláště při sportu nebo jiné pohybové aktivitě; glukosa je de facto lék na hypoglykémii. Pro některé lidské orgány, zejména pro mozek a červené krvinky, je glukosa zcela nezbytná. Je to jejich jediný zdroj energie, bez kterého se neobejdou. Tyto tkáně spotřebují za 24 hodin přibližně 150 g glukosy. To je tedy minimum, které musí zdravý člověk (ale i diabetik) přijmout, aby zabránil rozvoji katabolismu (tj. rozkládání složitějších látek na látky jednodušší) - získávání glukosy glukoneogenezí nebo ketogenezí (získávání energie za rozkladu mastných kyselin (Beta-oxidace); při tomto ději vznikají jako odpadní látky ketolátky, v prvé řadě aceton). Při poklesu hladiny glukosy (hypoglykémii) se ve žlázách s vnitřní sekrecí (pankreatu a nadledvinkách) začnou ihned uvolňovat kontraregulační hormony (glukagon a adrenalin), které mobilizují její tvorbu ze zásobního glykogenu (obsaženého převážně v játrech a ve svalstvu) procesem glykogenolýzy. Organismus nemá schopnost vytvořit glukosu z tuků vyjma velmi malého množství, které vzniká z glycerolu. Jako energetický zdroj je glukosa využívána i v umělé výživě (infuze) a její roztoky se podávají do žíly k zavodnění nemocných nebo jako nosiče pro jiné léky. Kaloricky je glukosa stejně vydatná jako cukr řepný, má však nižší sladivost, přibližně o 20 %. Z biochemického hlediska je aktivní formou D-glukosy D-glukosa-fosfát, vznikající z ní působením adenosin trifosfátu (ATP).
| Nutriční hodnoty (na 100 g) | |
| Využitelná energie | 1670 kJ |
| Sacharidy | 100 g |
| Bílkoviny | 0 g |
| Tuky | 0 g |
Koncentrace (hladina) D-glukosy v krvi se nazývá glykemie. Za běžných fyziologických podmínek získává organizmus glukosu:
- přísunem z vnějšího prostředí – potravou, ve formě buď samotné glukosy, či z disacharidů (sacharosa) popřípadě polysacharidů (škrob)
- z vlastních zásob – glykogenu, který je uložen zejména v játrech, ale i ve svalstvu. Tyto zásoby jsou omezené, činí od 150 do 400 g, podle situace, ve které se organizmus nalézá.
- glukoneogenezí z aminokyselin – tento zdroj je sice organizmu k dispozici, ale je velmi nevýhodný, protože bílkoviny jsou v organizmu jako strukturální látky, které mají svou pevně stanovenou funkci, a organizmus má velmi malé množství bílkovin, které sloužily pouze jako zásobní látky. Proto jakákoliv situace, kdy organizmus tvoří glukózu z aminokyselin, je pro něj výrazně nevýhodná.
Použití
Kromě již zmíněného použití v lékařství je surovinou pro fermentační výrobu ethanolu a alkoholických nápojů (pivo, víno atp.) alkoholovým kvašením působením kvasinek rodu Saccharomyces. Působením jiných mikroorganismů lze vyrábět i jiné důležité organické sloučeniny, jako butan-1-ol , glycerol, aceton, kyselinu mléčnou, kyselinu citronovou a j. Enzymaticky se z ní vyrábí mnohem sladší monosacharid fruktosa, používaná v potravinářském průmyslu.
| Náklady na energie a provoz naší encyklopedie prudce vzrostly. Potřebujeme vaši podporu... Kolik ?? To je na Vás. Náš FIO účet — 2500575897 / 2010 |
|---|
| Informace o článku.
Článek je převzat z Wikipedie, otevřené encyklopedie, do které přispívají dobrovolníci z celého světa. |