The final launch of the Allmultimedia.org will take place on February 27, 2026
(shortly after the 2026 Winter Olympics).
Bismut
Z Multimediaexpo.cz
m (1 revizi) |
m (1 revizi) |
Aktuální verze z 2. 12. 2013, 12:32
| Bismut | |
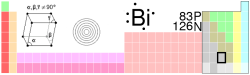
| |
| Atomové číslo | 83 |
| Relativní atomová hmotnost | 208,98040(1) amu |
| Elektronová konfigurace | [Xe] 4f14 5d10 6s2 6p3 |
| Elektronegativita (Pauling) | 2,02 |
| Teplota tání | 271,5 °C (544,7 K) |
| Teplota varu | 1564 °C (1837 K) |
| Hustota | 9,78 g.cm-3 |
| Hustota při teplotě tání | 10,05 g.cm-3 |
| Registrační číslo CAS | 7440-69-9 |
| Tvrdost | 2,25 |
Bismut (vizmut), chemická značka Bi, lat. Bismuthum patří mezi těžké kovy, které jsou známy lidstvu již od starověku. Slouží jako součást různých slitin, používá se při výrobě barviv a keramických materiálů.
Obsah |
Základní fyzikálně - chemické vlastnosti
Je těžký kovový prvek bílé barvy se slabým růžovým leskem, křehký a hrubě krystalický, známý již od starověku. V plynném stavu tvoří bismut molekuly Bi2. Na rozdíl od většiny ostatních těžkých kovů nejsou jeho sloučeniny toxické, vyskytuje se v nich v mocenství Bi+3 a méně často jako Bi+5.
Bismut se nerozpouští v neoxidujících kyselinách, protože je to ušlechtilý prvek. Snadno se však rozpouští především v kyselině chlorovodíkové za přítomnosti i malých množství oxidačních činidel (HNO3, H2O2, …). Bismut je na vzduchu za laboratorní teploty stálý, v červeném žáru shoří namodralým plamenem na oxid bismutitý Bi2O3, za žáru se bismut slučuje s většinou prvků. Bismut tvoří s většinou kovů slitiny, které mají nízké teploty tání.
Elementární bismut má největší diamagnetickou konstantu ze všech známých kovových prvků, značně vysoký elektrický odpor a vykazuje nejvyšší hodnotu Hallova efektu ze všech kovů. Společně se rtutí má nejnižší tepelnou vodivost ze známých kovových prvků.
Po dlouhou dobu byl bismut 209Bi pokládán za stabilní, neměnný izotop, přestože to odporovalo teoretickým výpočtům stability atomových jader. Teprve v roce 2003 byl francouzskými atomovými fyziky ve Výzkumném institutu astrofyziky v Orsay podán důkaz, že bismut podléhá radioaktivní přeměně. Bismut je tedy nestabilním prvkem, který podléhá alfa-rozpadu s poločasem přibližně 2×1019 let, což z něj činí jeden z nejpomaleji se přeměňujících přirozených radioizotopů.
Historický vývoj
- O bismutu jako o kovu podobném cínu se poprvé zmiňuje Baselius Valentinus v 15. století.
- Teprve v 18. století určili Pott a Bergman bismut jako zvláštní prvek kovového charakteru.
Výskyt
Bismut je v zemské kůře velmi vzácným prvkem. Průměrný obsah činí pouze 0,2 ppm (pars per milion; mg/kg). V mořské vodě činí jeho koncentrace pouze 0,017 mikrogramu v jednom litru. Předpokládá se, že ve vesmíru připadá na jeden atom bismutu přibližně 300 miliard atomů vodíku.
Bismut se v přírodě vyskytuje ryzí i ve sloučeninách. Hlavními minerály bismutu jsou bismutinit (psáno též bismutin), chemicky sulfid bismutitý Bi2S3, bismit jako oxid Bi2O3 a zásaditý uhličitan bismutit [(BiO) 2CO3]. Obvykle se vyskytuje jako příměs v rudách stříbra, zlata, cínu, mědi a olova.
U nás se rudy bismutu nalézají v Českosaském Rudohoří. Nejvíce bismutu těží Čína, Mexiko, Peru a Bolívie. Pouze bolivijská ložiska poskytují jako primární rudy minerály bismutu, v ostatních nalezištích tvoří bismut pouze příměsi v rudách jiných kovů.
Výroba
- Bismut byl ve starších dobách ze svých rud získáván vycezováním.
- Dnes se bismut za svých rud získává buď redukčním pochodem, kde bismit reaguje v peci s uhlíkem, nebo srážecím pochodem, kde se taví bismutinit se železem, popř. lze pražením převést sulfid na oxid a provést redukční pochod. Při těchto pochodech je bismut ještě značně znečištěn příměsemi, které byly v rudě, proto se surový bismut musí ještě rafinovat.
- Bi2O3 + 3 C → 2 Bi + 3 CO Redukční pochod
- Bi2S3 + 3 Fe → 2 Bi + 3 FeS Srážecí pochod
- 2 Bi2S3 + 9 O2 → 2 Bi2O3 + 6 SO2 Pražení sulfidu
- Pro získání velmi čistého bismutu lze využít elektrolýzu tavenin jeho sloučenin.
Využití
Významné uplatnění nalézá bismut jako legovaný prvek v různých slitinách.
Některé slitiny bismutu mají velmi nízký bod tání, často i pod bodem varu vody. Tohoto jevu se využívá při konstrukci automatických hasicích systémů (tzv. sprinklerů), které jsou montovány do výškových budov a automaticky začnou rozprašovat vodu při náhlém nárůstu teploty v okolí.
Vzhledem ke své nízké toxicitě se bismut stále častěji používá jako náhrada olova v nejrůznějších aplikacích – především jako složka pájek pro instalatérské práce, ale i při výrobě střeliva a broků.
Přídavek bismutu do slitin obvykle snižuje tvrdost materiálu a zvyšuje jeho kujnost. Slitina železa s bismutem je známa jako kujná litina a lze ji na rozdíl od běžné litiny snadno tvářet kováním i válcováním.
Slitiny bismutu obvykle při chladnutí mírně zvyšují svůj objem a slouží proto k lití do forem pro vytváření přesných replik a kopií různých předmětů. Bismut se používá do slitin ložiskových kovů. K známým nízkotajícím slitinám bismutu patří Woodův kov, který je směsí 55 % bismutu, 25 % olova, 15 % cínu a 5 % kadmia a taje okolo 70 °C. Lipowitzova slitina je směsí 50 % bismutu, 25 % olova, 15 % cínu a 10 % kadmia a teplotu tání má okolo 60 °C, je to nejníže tající slitina směsi těchto kovů. Roseův kov je směsí 50 % bismutu, 25 % olova a 25 % cínu a taje při 94 °C.
V chemickém průmyslu je bismut součástí katalyzátorů pro výrobu akrylátových vláken. Při výrobě keramiky slouží bismut jako náhrada olova při přípravě glazur, barviv pro keramické materiály a výrobě optických vlákem s vysokým indexem lomu. Bismut je důležitou součástí kosmetických a lékařských přípravků (např. v lékařství se používá zásaditá sůl kyseliny gallové Bi(OH)2·OCO·C6H2(OH)3 na zásyp ran - dermatol; sloučeniny bismutu se používají i jako léky proti sifilidě). Řada dalších různých sloučenin bismutu se používá v kosmetice a medicíně jako součást různých desinfekčních prostředků a léků používaných při léčení žaludečních a střevních chorob.
Slitina s manganem s názvem bismanol slouží pro výrobu velmi silných permanentních magnetů.
Sloučeniny
Ve sloučeninách se bismut vyskytuje především v mocenství Bi+3. Většina jeho solí je velmi málo rozpustná a snadno hydrolyzují.
- Oxid bismutitý Bi2O3 je za normální teploty žlutý a za horka červenohnědý prášek. Je to kyselinotvorný oxid. Vyskytuje se ve třech modifikacích. Připravuje se oxidací kovu nebo rozkladem dusičnanu či uhličitanu bismutitého.
- Chlorid bismutitý BiCl3 je sněhobílá krystalická látka, která se na vlhkém vzduchu rozplývá. Chlorid bismutitý totiž není stabilní a reaguje s vodou za vzniku oxichloridu bismutitého BiOCl, který se využívá jako netoxické barvivo známé jako perlová běloba.
- Bromid bismutitý BiBr3 a jodid bismuitý BiI3 jsou žluté prášky, které se vlastnostmi podobají chloridu bismutitému.
- Dusičnan bismutitý Bi(NO3)3 je bezbarvá krystalická rozpustná látka. Při zahřívání přechází na oxidusičnan bismutitý BiO(NO3), který se používá jako barvivo s názvem španělská běloba. Jiný zásaditý dusičnan bismutitý má využití v lékařství. Dusičnan bismutitý se připravuje rozpouštěním kovového bismutu v kyselině dusičné.
- Síran bizmutitý Bi2(SO4)3 je bílá krystalická, hygroskopická, rozpustná látka. Tvoří se rozpouštěním kovu, oxidu nebo sulfidu v kyselině sírové.
- Uhličitan bismutitý Bi2(CO3)3 je bílá práškovitá nerozpustná látka, která se připravuje reakcí rozpustné bismuité soli s rozpustným uhličitanem.
- Sulfid bismutitý Bi2S3 je tmavěhnědá (pokud se připravuje srážením se sirovodíkem) nebo šedá (pokud se připravuje tavením síry s bismutem) nerozpstná látka. Tmavěhnědý sulfid pozvolna přechází v šedou modifikaci. V přírodě se vyskytuje jako minerál bismutinit.
- Bismutovodík BiH3 neboli bismutan je bezbarvá, snadno se rozkládající plynná látka. Připravuje se (pouze v nepatrném výtěžku) při rozkladu práškové slitiny bismutu s hořčíkem kyselinou chlorovodíkovou.
Literatura a webové stránky
- Cotton F.A., Wilkinson J.:Anorganická chemie, souborné zpracování pro pokročilé, ACADEMIA, Praha 1973
- Holzbecher Z.:Analytická chemie, SNTL, Praha 1974
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood - A. Earnshaw, Chemie prvků 1. díl, 1. vydání 1993 ISBN 80-85427-38-9
- Periodická soustava a tabulka vlastností prvků [1]
- Chemický vzdělávací portál [2]
- WebElements (anglicky) [3]
- Periodická tabulka prvků [4]
|
| Náklady na energie a provoz naší encyklopedie prudce vzrostly. Potřebujeme vaši podporu... Kolik ?? To je na Vás. Náš FIO účet — 2500575897 / 2010 |
|---|
| Informace o článku.
Článek je převzat z Wikipedie, otevřené encyklopedie, do které přispívají dobrovolníci z celého světa. |


